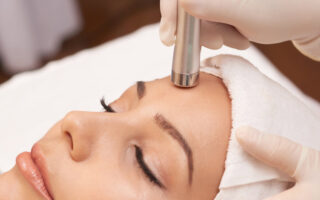
Skóra jest organem niezwykle złożonym. Składa się z trzech oddzielnych warstw: naskórka, skóry właściwej i tkanki podskórnej. Tkanka podskórna pełni rolę izolacyjną, to w niej odkłada, się większość tłuszczu, będącego zarówno materiałem zapasowym jak i chroniącym cały organizm przed zimnem i urazami mechanicznymi. Skóra właściwa jest oparciem dla całej konstrukcji, zapewnia wytrzymałość mechaniczną ale jej złe działanie zwłaszcza w starszym wieku prowadzi do zmarszczek i zmiany wyglądu. Naskórek, warstwa najbardziej zewnętrzna, odpowiada za wygląd skóry i wytwarza tzw. warstwę rogową, cieniutką martwą warstewkę będącą dzięki specyficznej budowie jedyną barierą, chroniącą nas przed wnikaniem mikroorganizmów i rozmaitych substancji z otoczenia. Zatrzymuje większość wody w naszym ciele, bez niej wyschlibyśmy na wiór. Warstwa rogowa zawdzięcza swoje właściwości obecności lipidów, dlatego nie przepuszcza wielu rozpuszczalnych w wodzie składników kosmetycznych jak np. cukry, aminokwasy, sole witamina C i wiele innych. Drugim czynnikiem ograniczającym wnikanie w skórę jest wielkość cząsteczki – niektóre są zbyt duże i „nie mieszczą się” pomiędzy substancjami obecnymi w warstwie rogowej. Dlatego w skórę nie wnikają żadne formy kolagenu i inne hydrolizaty protein, żadne przetwory Działa na powierzchni, nawilżająco kwasu hialuronowego chitozan i wie innych wielkocząsteczkowych substancji stosowanych w kosmetykach. Wszystkie zostają na powierzchni skóry tworząc warstwę działającą silnie nawilżająco. Można je wprowadzić w skórę, wymaga to jednak stosowania specjalnej aparatury: jontoforezy, ultradźwięków lub mezoterapii.
Tabela 1. Niektóre składniki kosmetyków NIE wnikające w skórę
| Surowiec kosmetyczny | Uwagi |
| Kolagen i jego hydrolizaty | Działają na powierzchni skóry, tylko nawilżająco |
| Kolagen rybi | Działa na powierzchni m skóry, tylko nawilżająco |
| Inne białka (proteiny) | Działają na powierzchni skóry, nawilżająco, niektóre mogą zmieniać właściwości skóry w dotyku |
| Hydrolizaty białek (protein) | Działają na powierzchni, skóry nawilżająco, niektóre mogą zmieniać właściwości skóry w dotyku |
| Kwas hialuronowy i jego hydrolizaty | Działają na powierzchni skóry, silnie nawilżająco |
| Chitozan | Działa na powierzchni skóry, nawilżająco |
| Silikony wielkocząsteczkowe | Działają na powierzchni skóry, nie wnikają, więc nie mogą szkodzić |
| Aminokwasy | Niektóre działają na powierzchni skóry, nawilżająco |
| Składniki NMF | Niektóre działają na powierzchni skóry, nawilżająco |
| Cukry | Niektóre działają na powierzchni skóry, nawilżająco |
| Sole mineralne | Sodu, potasu, wapnia, magnezu |
| Witamina C | Tylko wolna i sole |
| Witaminy z grupy B | Za wyjątkiem B5 – pantenolu |
| Składniki antyperspirantów | Główny składnik – sole glinu nie wnikają w skórę |
| Składniki samoopalaczy | Reagują chemicznie na powierzchni naskórka |
Tabela 2. Niektóre składniki kosmetyków wnikające w skórę
| Surowiec kosmetyczny | Uwagi |
| Oleje roślinne | Wnikają, ulegają przekształceniom, uwalniają kwasy tłuszczowe |
| Inne lipidy i składniki tłuszczopodobne | Wnikają, niektóre ulegają przekształceniom, uwalniają kwasy tłuszczowe |
| Olej parafinowy | Wnika tylko w warstwę rogową, nie penetruje dalej, nie może być szkodliwy |
| Sterole | Mogą pomagać w odbudowie bariery naskórkowej |
| Ceramidy i pseudoceramidy | Użyte w odpowiednim stężeniu mogą pomagać w odbudowie bariery naskórkowej |
| Alkohole tluszczowe | |
| Witamina A i jej pochodne | Palmitynian retinylu zatrzymuje się w warstwie rogowej uwalniany jest retinol, który przenika dalej |
| Witamina E i jej pochodne | Palmitynian tokoferylu zatrzymuje się w warstwie rogowej uwalnia tokoferol, która przenika dalej |
| Niektóre pochodne witaminy C | Np. palmitynian i fosforany |
| Flawonoidy | Przenikają ale powoli |
| Niskocząsteczkowe peptydy | Przenikają tylko te z zablokowanym końcem (pochodne) |
| Środki powierzchniowo czynne (ale nie wszystkie!) | Myjące, emulgatory, składniki płynów micelarnych, mogą ułatwiać wnikanie innych substancji |
| Kwas salicylowy | Usuwa zrogowacenia |
| Alfa-hydroksykwasy | Kwasy: glikolowy, mlekowy, cytrynowy i inne, nie wnikają w formie soli |
| Pantenol | Działa przeciwpodrażnieniowo |
| Gliceryna | Nawilża warstwę rogową również „od środka” |
| Glikol propylenowy | Nawilża warstwę rogową również „od środka” |
| Mocznik | Usuwa zrogowacenia |
Zgodnie z zasadami klasycznej farmakologii i toksykologii, działanie każdego związku biologicznie czynnego zależy od dwóch czynników: zdolności dotarcia do miejsca działania i wyzwolenia efektu fizjologicznego. Dotyczy to leków i innych substancji podawanych zewnętrznie na skórę lub błony śluzowe. W ich przypadku substancja czynna musi przeniknąć przez skórę. Po wniknięciu do krwioobiegu może przenikać do innych części organizmu i zależnie od właściwości wywoływać lokalne lub ogólne efekty fizjologiczne. Obszar docelowy większości leków podawanych zewnętrznie leży poza skórą. Tak działają m.in. leki przeciwzapalne czy estrogeny stosowane w formie plastrów przy hormonalnej terapii zastępczej. Efekty ich stosowania zależą w dużym stopniu od tego jak szybko substancja czynna przeniknie przez skórę i dostanie się do krwioobiegu. Starannie oceniana przez toksykologów ekspozycja (ilość substancji wnikającej do organizmu w wyniku kontaktu) zależy od szybkości przenikania. W tej sytuacji jest zrozumiałe, że podstawowym parametrem warunkującym efekt działania, tak leczniczy, jak i toksyczny jest zdolność do przeniknięcia przez skórę.
W przypadku substancji stosowanych w recepturach kosmetycznych sytuacja wygląda zupełnie inaczej.
W działaniu preparatów kosmetycznych główną rolę odgrywa tworzenie niewidocznego i niewyczuwalnego filmu na skórze. Mamy tu do czynienia z działaniem czysto fizycznym, bez jakiegokolwiek wnikania. Dla skóry skutki takiego działania są ogromne. Jest to m.in. wzrost ilości wody w naskórku (nawilżenie skóry) co ma decydujące znaczenie dla odnowy wierzchnich warstw i poprawia jej wygląd i zmniejsza podatność na czynniki drażniące i alergogenne.
Wiele substancji kosmetycznie czynnych działa na powierzchni skóry lub w martwej warstwie naskórka. Należą do nich m.in. filtry słoneczne, substancje ekranujące, większość substancji przeciwrodnikowych, hydroksykwasy, związki barwiące skórę i włosy i wiele innych. Tu problem wnikania w warstwę rogową staje się czynnikiem decydującym o skuteczności działania, dalsze przechodzenie do głębszych warstw skóry jest zdecydowanie niekorzystne, Składniki kosmetyków o działaniu quasi-farmakologicznym, takie jak np. witamina A i jej pochodne, witamina E, substancje przeciwpodrażnieniowe, niskocząsteczkowe peptydy, flawonoidy i inne substancje czynne pochodzenia roślinnego, powinny przenikać do żywych warstw naskórka i skóry właściwej. Skuteczność ich działania w dużym stopniu zależy od szybkości transportu w tkance skórnej – powinny stosunkowo łatwo przenikać przez warstwę rogową i następnie jak najwolniej rozprzestrzeniać się w żywej tkance, tak by zapobiec wnikaniu do krwioobiegu i odprowadzaniu do płynów ustrojowych. Osiągnięcie takiej dystrybucji jest praktycznie niemożliwe, dla większości substancji czynnych stosowanych w kosmetykach stężenie w żywych warstwach naskórka jest jedynie warunkowane szybkością przenikania przez warstwę rogową.
W literaturze problem biodostępności stosowanych zewnętrznie substancji czynnych jest traktowany w sposób uproszczony. Zdecydowana większość prac traktuje ten problem w sposób skrajny, stosując jedynie kryterium „zdolności do przenikania przez skórę”. Jest to w przypadku substancji kosmetycznie czynnych, zdecydowanie niewystarczające.
Do poczytania:
Banga, Ajay K.; Chien, Yie W. (1988): Iontophoretic delivery of drugs. Fundamentals, developments and biomedical applications. w: Journal of Controlled Release 7 (1), s. 1–24. DOI: 10.1016/0168-3659(88)90075-2.
Chandrasekaran, Navin Chandrakanth; Weir, Christopher; Alfraji, Sumaya; Grice, Jeff; Roberts, Michael S.; Barnard, Ross T. (2014): Effects of magnesium deficiency–more than skin deep. w: Experimental biology and medicine (Maywood, N.J.) 239 (10), s. 1280–1291. DOI: 10.1177/1535370214537745.
Dixit, Nitin; Bali, Vikas; Baboota, Sanjula; Ahuja, Alka; Ali, Javed (2007): Iontophoresis – an approach for controlled drug delivery: a review. w: Current drug delivery 4 (1), s. 1–10.
Dragicevic, Nina (red.) (2017): Drug penetration into/through the skin. Methodology and general considerations. Berlin, Heidelberg: Springer (Percutaneous penetration enhancers).
Dragicevic, Nina; Maibach, Howard I. (2015a): Chemical methods in penetration enhancement. Berlin: Springer (Percutaneous penetration enhancers).
Dragicevic, Nina; Maibach, Howard I. (2015b): Percutaneous penetration enhancers chemical methods in penetration enhancement. Berlin: Springer.
Ephrem, Elissa; Elaissari, Hamid; Greige-Gerges, Hélène (2017): Improvement of skin whitening agents efficiency through encapsulation: Current state of knowledge. w: International journal of pharmaceutics 526 (1-2), s. 50–68. DOI: 10.1016/j.ijpharm.2017.04.020.
Green, Barbara A.; Yu, Ruey J.; van Scott, Eugene J. (2009): Clinical and cosmeceutical uses of hydroxyacids. w: Clinics in dermatology 27 (5), s. 495–501. DOI: 10.1016/j.clindermatol.2009.06.023.
Green, Philip G. (1996): Iontophoretic delivery of peptide drugs. w: Journal of Controlled Release 41 (1-2), s. 33–48. DOI: 10.1016/0168-3659(96)01354-5.
Hatahet, T.; Morille, M.; Hommoss, A.; Devoisselle, J. M.; Müller, R. H.; Bégu, S. (2016): Quercetin topical application, from conventional dosage forms to nanodosage forms. w: European journal of pharmaceutics and biopharmaceutics : official journal of Arbeitsgemeinschaft fur Pharmazeutische Verfahrenstechnik e.V 108, s. 41–53. DOI: 10.1016/j.ejpb.2016.08.011.
Kemény, Lajos; Nagy, Nikoletta; Csoma, Zsanett; Szabó, Kornélia; Eros, Gábor (2016): Pharmacological Targeting of the Epidermal Barrier. w: CPD 22 (35), s. 5373–5381. DOI: 10.2174/1381612822666160726094947.
Münch, S.; Wohlrab, J.; Neubert, R. H. H. (2017): Dermal and transdermal delivery of pharmaceutically relevant macromolecules. w: European journal of pharmaceutics and biopharmaceutics : official journal of Arbeitsgemeinschaft fur Pharmazeutische Verfahrenstechnik e.V. DOI: 10.1016/j.ejpb.2017.06.019.
N’Da, David D. (2014): Prodrug strategies for enhancing the percutaneous absorption of drugs. w: Molecules (Basel, Switzerland) 19 (12), s. 20780–20807. DOI: 10.3390/molecules191220780.
Pai, Varadraj Vasant; Bhandari, Prasana; Shukla, Pankaj (2017): Topical peptides as cosmeceuticals. w: Indian journal of dermatology, venereology and leprology 83 (1), s. 9–18. DOI: 10.4103/0378-6323.186500.
Petry, T.; Bury, D.; Fautz, R.; Hauser, M.; Huber, B.; Markowetz, A. i wsp. (2017): Review of data on the dermal penetration of mineral oils and waxes used in cosmetic applications. w: Toxicology letters 280, s. 70–78. DOI: 10.1016/j.toxlet.2017.07.899.
Pharmaceutical skin penetration enhancement (op. 1993). New York: M. Dekker (Drugs and the pharmaceutical sciences, t. 59).
Phuong, Christina; Maibach, Howard I. (2016): Effect of massage on percutaneous penetration and skin decontamination: man and animal. w: Cutaneous and ocular toxicology 35 (2), s. 153–156. DOI: 10.3109/15569527.2015.1065501.
Priyanka, Karunanidhi; Singh, Sanjay (2014): A Review on Skin Targeted Delivery of Bioactives as Ultradeformable Vesicles. Overcoming the Penetration Problem. w: CDT 15 (2), s. 184–198. DOI: 10.2174/1389450115666140113100338.
Schoellhammer, Carl M.; Blankschtein, Daniel; Langer, Robert (2014): Skin permeabilization for transdermal drug delivery: recent advances and future prospects. w: Expert opinion on drug delivery 11 (3), s. 393–407. DOI: 10.1517/17425247.2014.875528.
Scott, R. C. (red.) (1990): Prediction of percutaneous penetration. Methods, measurements, modelling ; proceedings of the conference held in April, 1989. London: IBC Techn. Services.
Shah, Vinod P.; Maibach, Howard I. (1993): Topical drug bioavailability, bioequivalence, and penetration. New York: Plenum Press.
Skin Permeation and Disposition of Therapeutic and Cosmeceutical Compounds (2018): Springer Verlag.
Tsakovska, Ivanka; Pajeva, Ilza; Al Sharif, Merilin; Alov, Petko; Fioravanzo, Elena; Kovarich, Simona i wsp. (2017): Quantitative structure-skin permeability relationships. w: Toxicology 387, s. 27–42. DOI: 10.1016/j.tox.2017.06.008.
Tyle, P. (1986): lontophoretic Devices for Drug Delivery. w: Pharmaceutical research 3 (6), s. 318–326. DOI: 10.1023/A:1016327822325.
Verallo-Rowell, Vermén M.; Katalbas, Stephanie S.; Pangasinan, Julia P. (2016): Natural (Mineral, Vegetable, Coconut, Essential) Oils and Contact Dermatitis. w: Current Allergy and Asthma Reports 16 (7), s. 51. DOI: 10.1007/s11882-016-0630-9.
Walters, Kenneth A. (1993): Pharmaceutical skin penetration enhancement. New York u.a.: Dekker (Drugs and the pharmaceutical sciences, t. 59).
Link do artykułu na blogu file:///C:/Users/Beauty%20Up/Desktop/3PdgZlWf.htm